- Symptome des Keratokonus
- Therapie des Keratokonus (Entwicklung)
- Therapie des Keratokonus (Therapieschema zentrumsehstärke)
Keratokonus Zentrum Hamburg (Übersicht)
Durch die langjährige klinische und wissenschaftliche Erfahrung unserer medizinischen Leiter Prof. Dr. med. Stephan Linke und Privatdozent Dr. med. Johannes Steinberg, FEBO, sowie unsere apparative Ausstattung im Bereich Diagnostik und Therapie, sind wir Norddeutschlands Referenzzentrum im Bereich Keratokonus Behandlung und Therapie.
Auszug aus der Habilitationsschrift von Priv.-Doz. Dr. Johannes Steinberg (2014)
Der Keratokonus ist eine progressive, beide Augen asymmetrisch betreffende, nichtentzündliche Hornhauterkrankung, welche durch eine zunehmende Verformung und Verdünnung des Gewebes charakterisiert ist [13]. Die dabei charakteristischerweise auftretende zentrale oder parazentrale Vorwölbung der Hornhaut führt zu einer Veränderung der Lichtbrechung (Refraktion), welche sich klinisch in einer zunehmenden Kurzsichtigkeit (Myopie) bzw. einer progressiven irregulären Hornhautverkrümmung (Astigmatismus) zeigt. Durch eine zunehmende Veränderung der kollagenen Mikrostruktur der Hornhaut kommt es in den fortgeschrittenen Stadien u.a. zu einer Verdünnung der Hornhaut mit Narbenbildung bis hin zu akuten Wassereinlagerungen im Gewebe (Hydrops) auf Grund von spannungsbedingten Rissen der Descemet-Membran.
Über die genauen Ursachen und Auslöser des Keratokonus sind bis zum heutigen Tage wenig bekannt. Histologische Studien konnten als ursächlich für die morphologischen Veränderungen eine Verminderung und unregelmäßige Anordnung der kornealen Kollagenlamellen, eine veränderte Verteilung der Kollagentypen sowie extrazelluläre Matrixveränderungen der Proteoglykane im Hornhautstroma nachweisen [14-16]. Die Tatsache, dass erstgradige Verwandte eine deutlich höhere Wahrscheinlichkeit für die Erkrankung aufweisen und monozygote Zwillinge hohe phänotypische Übereinstimmungen in der Ausprägung der Erkrankung aufweisen, lassen eine hereditäre Ursache sehr wahrscheinlich erscheinen [17-19]. Dennoch wird nach wie vor einer Großzahl der Neuerkrankungen ein sporadisches, nicht hereditäres Auftreten zugeschrieben [20]. Molekulargenetisch konnte kein singulärer Gen-Defekt als ursächlich aufgezeigt werden. Vielmehr wurden bis zum heutigen Tage Veränderungen an 17 Genloci als ursächlich für die Entstehung des Keratokonus identifiziert [20]. Daher, und auf Grund häufiger Assoziationen mit generalisierten Erkrankungen (u.a. atopische Diathese, Trisomie 21) sowie unterschiedlichen Prävalenzen in verschiedenen Ethnizitäten, geht man heutzutage von einer multifaktoriellen Genese der Erkrankung aus [20, 21].
Weltweit betrachtet liegt die Inzidenz bei ca. 1/2000, wobei starke Unterschiede hinsichtlich der Ethnizitäten nachgewiesen werden konnten (z.B. relative Inzidenz Europäer : Asiaten = 1:4,4 [22] bis 1:9 [23]). Die Angaben zum mittleren Alter bei der Diagnose variieren in der Literatur zwischen im Mittel 24-27 Jahre. Die Erkrankung lässt sich jedoch in vielen Fällen bereits im Teenager-Alter diagnostizieren und weist gerade bei jüngeren Betroffenen in der Regel eine stärkere Dynamik auf als bei älteren Patienten [24].



Symptome des Keratokonus
Die ersten, vom Patienten zu bemerkenden Symptome sind in der Regel eine leichte Sehunschärfe und in einigen Fällen eine zunehmende Lichtempfindlichkeit gerade beim Betrachten von künstlichen Lichtquellen im Dunkeln (z.B. die Autoscheinwerfer bei Nacht).
Wenn die Verformung der Hornhaut zunimmt, bemerkt man in der Regel eine zunehmende Sehunschärfe da die zunehmende Vorwölbung und Verziehung der Hornhaut zu einer zunehmenden Kurzsichtigkeit und unregelmäßigen Hornhautverkrümmung (Astigmatismus) führt. Sich innerhalb von wenigen Monaten verändernde Brillenwerte und eine nicht voll erreichbare Sehschärfe auch mit der neu angepassten Brille sind späte „Alarmsymptome“. Die Erkrankung ist typischerweise unterschiedlich stark in den beiden Augen ausgeprägt, so dass Betroffene einen zunehmenden Unterschied zwischen den Augen bzgl. der geschilderten Symptome wahrnehmen.
Typische, häufige Symptome von Keratokonus-Patieten:
-Gestörter Seheindruck mit/ ohne Brille in Nähe und Ferne
-Einäugig betonte Symptome
-„Geisterbilder“ (–> Wahrnehmung von mehreren Bildern/ Bilddopplungen beim Betrachten eines Objektes)
-Schattenbildung typischerweise in Form eines Kometenschweifs beim Betrachten von Objekten/ Buchstaben
-Schlechte Nachtsicht durch vermehrte Blendempfindlichkeit im Dunkeln
-Zunehmende Lichtempfindlichkeit (durch Streuung des Lichtes)
Therapie des Keratokonus (Entwicklung)
Auszug aus der Habilitationsschrift von Priv.-Doz. Dr. Johannes Steinberg (2014)
Neben dem Anpassen refraktiver Korrekturmöglichkeiten (Brille, formstabile Kontaktlinse) in den frühen Stadien, stellte die Hornhauttransplantation jahrzehntelang die einzige operative Therapie des Keratokonus und Ultima Ratio zugleich dar [21].
In den letzten Jahren haben besonders vier Entwicklungen zu einem vermehrten Interesse im Bereich der Keratokonusforschung beigetragen:
I) Seit der ersten Laser in situ Keratomileusis (LASIK) in den frühen 90er Jahren wurden insbesondere in den letzten zwei Jahrzehnten deutliche Fortschritte in dem Bereich der refraktiven Hornhautchirurgie erzielt [25]. Mit weltweit mehr als 40 Millionen Eingriffen stellt die LASIK mittlerweile das am häufigsten angewandte operativen Verfahren am Menschen dar (Market Scope, 2013). Der Keratokonus gilt als eines der wenigen absoluten Ausschlusskriterien der LASIK [2, 26]. Bei jeder LASIK oder vergleichbaren kornealen refraktiven Verfahren wird auf Grund des Gewebsabtrages die Biomechanik der Hornhaut geschwächt. Bereits ein geringer Gewebsabtrag bei Menschen mit einem Keratokonus können selbst bei zuvor minimaler bis nicht diagnostizierbarer Ausprägung der Erkrankung zu post-LASIK-Ektasien mit potentiell verheerenden refraktiven Ergebnissen führen [2, 26].
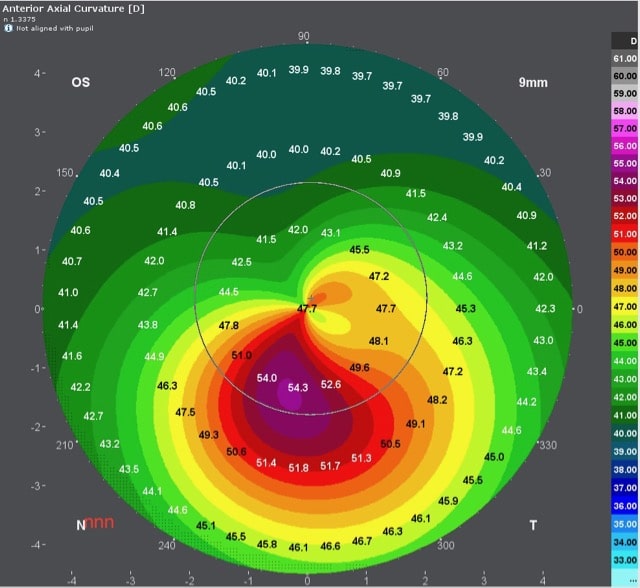
II) Die deutliche Zunahme der korneal-refraktiven Eingriffe hat besonders im letzten Jahrzehnt auch zu einer starken Weiterentwicklung der Diagnoseverfahren der Hornhaut geführt. Während bis zum Beginn des Jahrtausends die Analyse der Hornhautoberfläche (Topographie) als sensitivstes Verfahren zur Früherkennung des Keratokonus galt [12, 27, 28], ermöglichten es neue Technologien, in-vivo und kontaktfrei innerhalb von wenigen Sekunden die gesamte morphologische Hornhautstruktur (Tomographie), die punktspezifische Lichtbrechung der Hornhaut über deren gesamte Fläche (Wellenfrontanalysen), sowie deren biomechanischen Eigenschaften hochauflösend und reproduzierbar zu analysieren [29-37].
III) Seit dem Jahr 2003 steht mit der Hornhautquervernetzung erstmalig ein potentes Therapieverfahren zur Verfügung, welches einen Stopp der Progression des Keratokonus ermöglichen kann [38]. Vermittelt durch eine UV-Bestrahlung und katalysiert durch Riboflavin-haltigen Augentropfen kommt es zu einer vermehrten Sauerstoffradikalfreisetzung im Gewebe und als Folge zu einer photooxidativen Quervernetzung. Dies führt, durch Restrukturierungen innerhalb des Hornhautgewebes, zu einer „Verhärtung“ und somit zu einer zunehmenden Stabilisierung der Hornhaut. Mittels der Hornhautquervernetzung (auch Crosslinking genannt), kann somit eine Stabilisierung der Hornhautform erzielt werden. Da dies jedoch nicht gleichzeitig zu einer Regularisierung der Hornhautform bzw. Sehverbesserung führt, ist dieses Verfahren nur bei Patienten mit noch guter Sehfähigkeit und/ oder guter Kontaktlinsen-Verträglichkeit sinnvoll.
IV) Seit 2008 besteht die Möglichkeit, mittels eines geschlossenen Ringsystems (MyoRing, CISIS), welches direkt in die Hornhaut eingesetzt wird, diese zu stabilisieren und hinsichtlich ihrer Form zu regularisieren. Damit stellen die MyoRinge zu Zeit das einzige Therapieverfahren des Keratokonus dar, welches sowohl einen Progressionsstopp, als auch eine Sehverbesserung (mit + ohne Brillen-/ Kontaktlinsen-Korrektur) ermöglichen kann.
 MyoRing zentral in der Hornhaut (Übersichtsdarstellung mittels Spaltlampe)
MyoRing zentral in der Hornhaut (Übersichtsdarstellung mittels Spaltlampe)
Therapie des Keratokonus (Therapieschema zentrumsehstärke – Hamburg)
(Vorgehen im zentrumsehstärke)
Beim Erstkontakt/ bei der Erstdiagnose des Keratokonus sind u.a. 2 Aspekte des Patienten/ der Hornhaut wichtig:
I) Liegt eine gute Sehfähigkeit mit Brillen- und/ oder Kontaktlinsenkorrektur vor?
II) Ist der Befund stabil, oder liegt eine Progression (zunehmende Verformung der Hornhaut) vor?
Bei einer guten Sehfähigkeit wird in der Regel eine Versorgung mittels Brillengläsern und/ oder Kontaktlinsen empfohlen. Die Kontaktlinsen sind ab einem bestimmten Grad der Erkrankung eher in der Lage die Sehfehler auszugleichen als die Brillengläser (Wenn die Hornhaut bereits sehr unregelmäßig verzogen ist, ist die auf der Hornhaut „schwimmende“ Kontaktlinse besser in der Lage die Unregelmäßigkeiten auszugleichen und somit Lichtbrechungsstörphänomene zu korrigieren). Da die Erkrankung in Schüben verlaufen kann, werden Kontrolltermine vereinbart an denen die Hornhaut gescannt, die Brillenstärke überprüft und die Sehstärke des Patienten getestet wird. Wenn der Befund stabil ist, führen wir in der Regel keine operative Therapie durch. Ausnahmen können z.B. sehr junge Patienten sein (Teenager) bei denen ein deutlich höheres Risiko für eine Progression besteht als bei „älteren“ Keratokonuspatienten über 40.
Sehr wichtig für alle Patienten mit Keratokonus ist: Reiben Sie nicht Ihre Augen.
Die Theorie, dass das Reiben der Augen nach wie vor einer der wichtigsten Verstärkungsfaktoren, ggf. sogar entscheidender Auslöser/ Unterhalter der Erkrankung ist, hält sich nach wie vor. Solange wir Ärzte nicht sicher wissen, was die Erkrankung auslöst, bitte: REIBEN SIE NICHT IHRE AUGEN.
(Für Interessenten haben wir hier weitere (englischsprachige Informationen zum Thema Augenreiben und Keratokonus):
No Rub, no cone (damien gatinel)
Eine Kontroverse Diskussion zu dem Thema finden Sie zudem unten auf dieser Seite (Youtube – Link).
Ist der Befund bei guter Sehfähigkeit progressiv, führen wir hier in Hamburg entsprechend der aktuellen Studienlage zeitnah eine Stabilisierungstherapie des Keratokonus (Hornhautquervernetzung/ „Crosslinking“) durch um den Befund im optimalen Befund „einzufrieren“/ eine weitere Verformung der Hornhaut zu verhindern.
Bei einer nicht ausreichenden Sehschärfe und/ oder Progression besteht in Hamburg die Möglichkeit über die Implantation eines geschlossenen Ringsystems in die Hornhaut (CISIS/ MyoRing) diese zu stabilisieren und zu regularisieren. Durch die Regularisierung der zuvor irregulären („verzogenen“) Hornhaut ist in der Regel eine Verbesserung des Sehens ohne, vor allem aber mit Brille, ggf. auch mit anschließend erneutem Tragen von Kontaktlinsen (weichen oder besser verträglichen formstabilen oder Hybrid-Linsen) möglich.
Alternativ ist es bei einigen Patienten auf Grund der Ausgangsbrillenwerte und Lokalisation des Konus sinnvoller eine Hornhautquervernetzung mit einer Laserbehandlung der Hornhaut zur Regularisierung + gleichzeitigen Verstärkung durchzuführen.
Dies ist jedoch nur bei sehr geringen Verformungen der Hornhaut sinnvoll, da die Laserbehandlung unweigerlich zu einem Antrag von Hornhautgewebe führt, was die Hornhaut per se schwächt. Zwar ist dies in Kombination mit einer „Verhärtung“ der Hornhaut (Hornhautquervernetzung) möglich, jedoch nur bei geringem Hornhautgewebsabtrag.
Sind stärkere „Umformungen“ der Hornhaut erforderlich um sie in eine ausreichend reguläre Form zu bringen, setzen wir Hornhautimplantate ein. Diese Implantate sind, je nach Verfügbarkeit, aus Kunststoff, wenn möglich jedoch mittlerweile überwiegend aus Spendermaterial verstorbener Menschen (Corneal Allogenic Intrastromal Ring Segments, CAIRS). Die Implantation von Ringsegmenten ist, je nach Fall, kombinierbar mit einer Hornhautquervernetzung oder einer Transplantation einer dünnen, stabilisierenden Hornhautschicht (Bowman-Schicht-Transplantation).
Die Entscheidung welche Therapie eine möglichst gute Sehfähigkeit bei Erhalt der Hornhaut ermöglichst ist nur sehr individuell basierend auf der Situation des jeweiligen Patienten/-in zu treffen. Also grobe Orientierung dient uns folgendes Schema:
Bei Progression des Keratokonus und/ oder Ziel der Sehverbesserung:
Athen Protokoll (Laserbehandlung + Quervernetzung):
-frühes Stadium des Keratokonus
-leichte Kurzsichtigkeit (Myopie); Weitsichtigkeit (Hyperopie)
-Bestkorrigierter Visus (Sehstärke) <0.7
-Minimale Hornhautdicke >=400 Mikrometer
Intrakorneale Ringsegmente (CAIRS) (+ ggf. Quervernetzung) oder Bowman-Schicht-Transplantation oder Kombination CAIRS + Bowman-Schicht-Transplantation
-fortgeschrittenes Stadium des Keratokonus
-Bestkorrigierter Visus (Sehstärke) <0.5
-Minimale Hornhautdicke >=400 Mikrometer
Ist der Keratokonus zu weit fortgeschritten (Narbenbildung, Hornhautdicke < 350 Mikrometer) ist eine hornhauterhaltende Therapie in der Regel nicht mehr sinnvoll, so dass wir den operativen Austausch der Hornhaut („Hornhauttransplantation“) empfehlen und mit den Patienten diskutieren. Tiefe-Schichten-Transplantationen führen wir ebenfalls in unseren OPs durch. Sollte auch dies nicht mehr sinnvoll für den Patienten/-in sein, da z.B. zentrale Narben durch das ganze Hornhautgewebe reichen, ist teilweise „nur“ eine vollständige Transplantation der Hornhaut sinnvoll um auf eine verbesserte Sehleistung zu kommen. Die vollständige Transplantation führen wir nicht im zentrumsehstärke durch. Wir verweisen in den Fällen jedoch gerne auf Kollegen in Universitätskliniken zur weiteren Versorgung.
Ein Beispiel dafür, dass die Erkrankung dennoch Spitzenleistungen möglich macht, sind die von uns behandelten ärztlich-chirurgischen Kollegen, von uns behandelte Piloten und auch internationale Sport Stars wie Stephen Curry, einem der besten, wenn nicht der Beste Distanzschütze in der NBA-Geschichte. Ein kurzer Artikel zu seiner Erkrankung finden Sie unter diesem Link.
Quellen:
12) Rabinowitz, Y.S. and K. Rasheed, KISA% index: a quantitative videokeratography algorithm embodying minimal topographic criteria for diagnosing keratoconus. J Cataract Refract Surg, 1999. 25(10): p. 1327-35.
13) Krachmer, J.H., R.S. Feder, and M.W. Belin, Keratoconus and related noninflammatory corneal thinning disorders. Surv Ophthalmol, 1984. 28(4): p. 293-322.
14) Akhtar, S., et al., Ultrastructural analysis of collagen fibrils and proteoglycans in keratoconus. Acta Ophthalmol, 2008. 86(7): p. 764-72.
15) Hayes, S., et al., Depth profile study of abnormal collagen orientation in keratoconus corneas. Arch Ophthalmol, 2012. 130(2): p. 251-2.
16) Meek, K.M., et al., Changes in collagen orientation and distribution in keratoconus corneas. Invest Ophthalmol Vis Sci, 2005. 46(6): p. 1948-56.
17) Kennedy, R.H., W.M. Bourne, and J.A. Dyer, A 48-year clinical and epidemiologic study of keratoconus. Am J Ophthalmol, 1986. 101(3): p. 267-73.
18) Rabinowitz, Y.S., The genetics of keratoconus. Ophthalmol Clin North Am, 2003. 16(4): p. 607-20, vii.
19) Tuft, S.J., et al., Keratoconus in 18 pairs of twins. Acta Ophthalmol, 2012. 90(6): p. e482-6.
20) Abu-Amero, K.K., A.M. Al-Muammar, and A.A. Kondkar, Genetics of keratoconus: where do we stand? J Ophthalmol, 2014. 2014: p. 641708.
21) Buhren, J., G. Bischoff, and T. Kohnen, [Keratoconus: clinical aspects, diagnosis, therapeutic possibilities]. Klin Monbl Augenheilkd, 2011. 228(10): p. 923-40; quiz 941-2.
22) Pearson, A.R., et al., Does ethnic origin influence the incidence or severity of keratoconus? Eye (Lond), 2000. 14 ( Pt 4): p. 625-8.
23) Georgiou, T., et al., Influence of ethnic origin on the incidence of keratoconus and associated atopic disease in Asians and white patients. Eye (Lond), 2004. 18(4): p. 379-83.
24) Tuft, S.J., et al., Prognostic factors for the progression of keratoconus. Ophthalmology, 1994. 101(3): p. 439-47.
25) Reinstein, D.Z., T.J. Archer, and M. Gobbe, The history of LASIK. J Refract Surg, 2012. 28(4): p. 291-8.
26) Tatar, M.G., et al., Risk Factors in Post-LASIK Corneal Ectasia. J Ophthalmol, 2014. 2014: p. 204191.
27) Maeda, N., et al., Automated keratoconus screening with corneal topography analysis. Invest Ophthalmol Vis Sci, 1994. 35(6): p. 2749-57.
28) Rabinowitz, Y.S., Videokeratographic indices to aid in screening for keratoconus. J Refract Surg, 1995. 11(5): p. 371-9.
29) Ambrosio, R., Jr. and M.W. Belin, Imaging of the cornea: topography vs tomography. J Refract Surg, 2010. 26(11): p. 847-9.
30) Ambrosio, R., Jr., et al., Novel pachymetric parameters based on corneal tomography for diagnosing keratoconus. J Refract Surg, 2011. 27(10): p. 753-8.
31) Ucakhan, O.O., et al., Evaluation of Scheimpflug imaging parameters in subclinical keratoconus, keratoconus, and normal eyes. J Cataract Refract Surg, 2011. 37(6): p. 1116-24.
32) Ahmadi Hosseini, S.M., et al., Corneal thickness and volume in subclinical and clinical keratoconus. Int Ophthalmol, 2013. 33(2): p. 139-45.
33) de Sanctis, U., et al., Diagnosis of subclinical keratoconus using posterior elevation measured with 2 different methods. Cornea, 2013. 32(7): p. 911-5.
34) Jafarinasab, M.R., et al., Evaluation of corneal elevation in eyes with subclinical keratoconus and keratoconus using Galilei double Scheimpflug analyzer. Eur J Ophthalmol, 2013. 23(3): p. 377-84.
35) Muftuoglu, O., et al., Posterior corneal elevation and back difference corneal elevation in diagnosing forme fruste keratoconus in the fellow eyes of unilateral keratoconus patients. J Cataract Refract Surg, 2013. 39(9): p. 1348-57.
36) Ali, N.Q., D.V. Patel, and C.N. McGhee, Biomechanical responses of healthy and keratoconic corneas measured using a non contact Scheimpflug tonometer. Invest Ophthalmol Vis Sci, 2014.
37) Bae, G.H., et al., Corneal topographic and tomographic analysis of fellow eyes in unilateral keratoconus patients using Pentacam. Am J Ophthalmol, 2014. 157(1): p. 103-109 e1.



